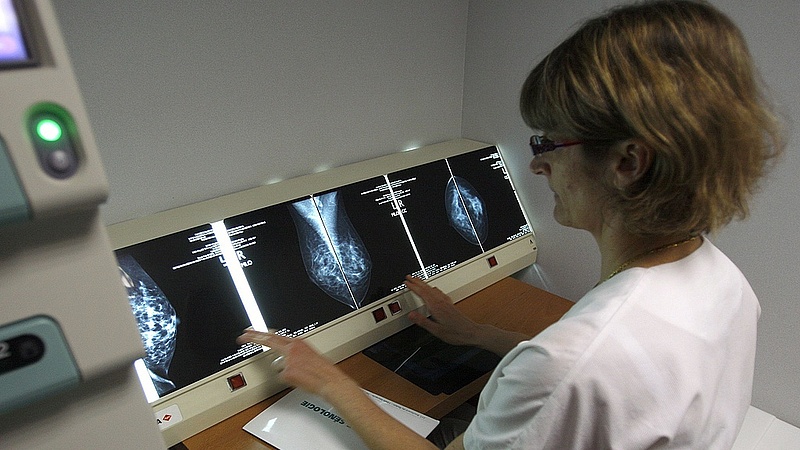
November elsejétől változhat a gyógyszerfinanszírozás, az intézkedések jelentősen szűkíthetik az innovatív onkológiai terápiák elérhetőségét - értesült a Magyar Narancs. Információik szerint a módosítás lényege, hogy az innovatív onkológiai gyógyszerek esetében is bevezetnék a vaklicitet, azaz azt az eljárást, amelynek során az OEP utódja, a Nemzeti Egészségbiztosítási Alapkezelő (NEAK) árajánlatot kér a gyógyszergyártóktól, s a győztes a legalacsonyabb árat ajánló gyártó lesz, azaz ezt a gyógyszert fogadja be a NEAK a támogatási rendszerbe.
A vaklicitet eddig nem alkalmazták innovatív készítményekre, csak olyanokra, amelyeket az eredeti (innovatív) gyógyszerek szabadalmi védettsége után, azonos hatóanyagból más gyártók rendszerint olcsóbban állítottak elő. Az eljárás célja egyértelműen az azonos hatóanyagú (hatású) gyógyszerek közül a legolcsóbb kiválasztása, csupán ezzel a lépéssel tízmilliárdokat spóroltak meg a gyógyszerkasszán a vaklicit indulása óta. Noha a vaklicit gazdasági haszna - főleg a bevezetést követő időszakban - nem volt kérdéses, szakmai alapon azonban több támadás érte a rendszert, a tapasztalatok szerint ugyanis azonos hatóanyag - tehát elvileg teljes helyettesíthetőség - mellett sem sikerül mindig ugyanazt a hatást kiváltani, a generikumok eltérő mellékhatásairól nem is beszélve.
Kapcsolódó
Önmagában az a célkitűzés, hogy az onkológiai gyógyszereket olyan új rendszerbe sorolják, amelyben a költséghatékonyságot is figyelembe veszik, akár helyesnek is tekinthető - kommentálta a hírt lapunk kérdésére Poller Imre onkológus. Az innovatív onkológiai terápiák esetében viszont súlyos hiba volna kizárólag gazdasági alapon szelektálni.
Hatóanyag vagy hatásterület
Az intézkedés értékelésének kulcskérdése, hogy az onkológiai gyógyszereket érintő tenderkiírásban hatóanyagot vagy hatásterületet határoznak meg, és ha az utóbbit, akkor a hatás felmérésében milyen tapasztalatokra támaszkodnak, milyen szempontok alapján minősítik azt - magyarázza a szakértő.
Poller szerint a korszerű onkológiai terápiák esetében eleve helyesebb megközelítés a hatásterület meghatározása. A személyre szabott orvoslásban egyre inkább előretörő, genetikai háttérre alapozott biológia terápiák ugyanis többféle hatóanyaggal, és többféle támadásponton avatkoznak be egy-egy speciális daganatos betegség alakulásába. Ami azt jelenti, hogy a hatóanyag alapon kiírt tender esetén alapból kiesik számos gyógyszer, amely potenciálisan ugyanolyan jól és nem drágábban, vagy akár költséghatékonyabban kezelhet hasonló onkológiai betegségeket.
Könnyű mellékvágányra futni
Ugyanakkor könnyű mellékvágányra futni akkor is, ha a hatásterületet célozza meg a kiírás - hívja fel a figyelmet Poller Imre. Ebben az esetben az vezet tévútra, ha a szakmai és gazdaságossági szempontok közül az egyiket preferálják, vagy kizárólag az alapján döntenek. A pusztán az árat pontozó döntésnél előnyt élvezhet egy olyan biohasonló gyógyszer, amely adott hatásterületen ugyan olcsóbb egy másik, biológiai válaszmódosító gyógyszernél, de annál rövidebb idejű túlélést ígér a tapasztalatok alapján.
A szakmai szempontok értékelését is árnyalni érdemes, és nem csak a gyógyszerkassza fenntarthatósága érdekében. Az innovatív onkológiai gyógyszerek, azaz a biológiai terápiák hatását nemzetközi klinikai kipróbálás során, nagy populáción vizsgálják, az amerikai gyógyszergyárak például jellemzően Európában. De arra is van példa, hogy ázsiai betegeken végzik a klinikai fázis vizsgálatokat olyan gyógyszerek esetében, amelyeket aztán Európában, vagy az amerikai kontinensen készülnek alkalmazni.
Az ártalmak jellemzően ezeken a próbákon kiszűrhetőek, azonban a populáció genetikai eltérései miatt sokszor nem ugyanazt a gyógyhatást produkálják a készítmények a célközönségnél, mint ahol a klinikai vizsgálatokat végezték. Az onkológiában is terjedő úgynevezett biohasonló gyógyszerek esetében - ezeknek ugyanaz a hatásterülete, mint az innovatív biológiai terápiáknak, de más a hatóanyag, és más a gyógyszer konkrét támadáspontja, ahol beavatkozik a daganatsejt életébe - rendszerint kisebb körben, akár csak egy-egy kórházban próbálják ki a készítményt. Ez egy olyan terület, ahol az innovatív és a generikus gyógyszergyártás szinte egymásba mosódik, és nem lehet mindenre érvényes döntést hozni, szinte készítményenként kell elemzést végezni.
Ne csak azt bizonyítsák, hogy nem árt
A kétezres évek végén volt is botrány belőle, amikor egy olyan biohasonló gyógyszer került be majdnem az országos támogatási rendszerbe, amelyet alig negyven betegen próbáltak ki egyetlen balkáni ország kórházában, és ott is igazából csak az derült ki, hogy a gyógyszer nem ártalmas - idéz fel egy esetet Poller Imre.
Még ha a költséghatékonyság is a legfőbb cél, akkor is elengedhetetlen az ár mellett a már összegyűlt hazai szakmai tapasztalatokat figyelembe venni. Fontos volna, hogy az eddigi hazai alkalmazás gyakorlati tapasztalatainak objektív elemzése is rendelkezésre álljon a vaklicit értékelésnél, illetve azok a gyógyszerek, amelyek a törzskönyvük alapján széleskörű nemzetközi vizsgálati eredményekkel és tapasztalatokkal rendelkeznek, semmiképpen ne essenek ki a körből már a tenderkiírás pillanatában - hangsúlyozta a szakértő.
DeGiro
A hihetetlenül alacsony tarifák és az elégedett ügyfelek véleményei révén a DEGIRO a leggyorsabban növekvő bróker Európában. Regisztráljon, és fektessen be a DEGIRO biztonsági struktúráján keresztül.